Regulatory Affairs

PRRC: Verantwortliche Person in Medizintechnik-Unternehmen
Artikel 15 der MDR 2017/745 (EU) fordert, dass jeder Hersteller mindestens eine Verantwortliche Person oder auch PRRC (Person Responsible for Regulatory Compliance) in seinem Unternehmen benennt.
Verantwortlichen Person: Wer übernimmt die Aufgabe?
Neben den Herstellern benötigen auch EU-Bevollmächtigte und andere Wirtschaftsakteure, die Herstellerpflichten übernehmen, eine Verantwortliche Person in ihrem Unternehmen. Ausgenommen davon sind Klein- und Kleinstunternehmen, die auch auf eine externe verantwortliche Person zurückgreifen dürfen, sofern der dauerhafte und ständige Zugriff auf diese Person gewährleistet ist. Die Verantwortliche Person muss ihre Qualifikation für die Einhaltung der relevanten Regulierungsvorschriften über ein Hochschulstudium und mindestens 1 Jahr relevante Berufserfahrung oder mindestens 4 Jahre relevante Berufserfahrung nachweisen.
Aufgaben der Verantwortlichen Person
Der Verantwortlichen Person obliegt die Zuständigkeit für verschiedene Bereiche. Gemäß Artikel 15 zählen dazu mindestens:
- Produktkonformität und Produktfreigabe
- Erstellung und Aktualisierung von Technischer Dokumentation und EU-Konformitätserklärung
- Überwachung nach dem Inverkehrbringen
- Berichtspflichten bezüglich der Meldung von schwerwiegenden Vorkommnissen und Sicherheitskorrekturmaßnahmen im Feld
- Überprüfung der Abgabe einer Erklärung im Falle von Prüfprodukten
Die MDR regelt ebenfalls, dass die korrekte Wahrnehmung ihrer Verantwortungen und Pflichten der Verantwortlichen Person keinen Nachteil bringen darf.
Herausforderung für Hersteller und EU-Repräsentanten
Die MDR legt zwar die Verantwortlichkeiten fest, lässt dabei aber offen, wie die Verantwortliche Person ihren Verpflichtungen praktisch nachkommen soll.
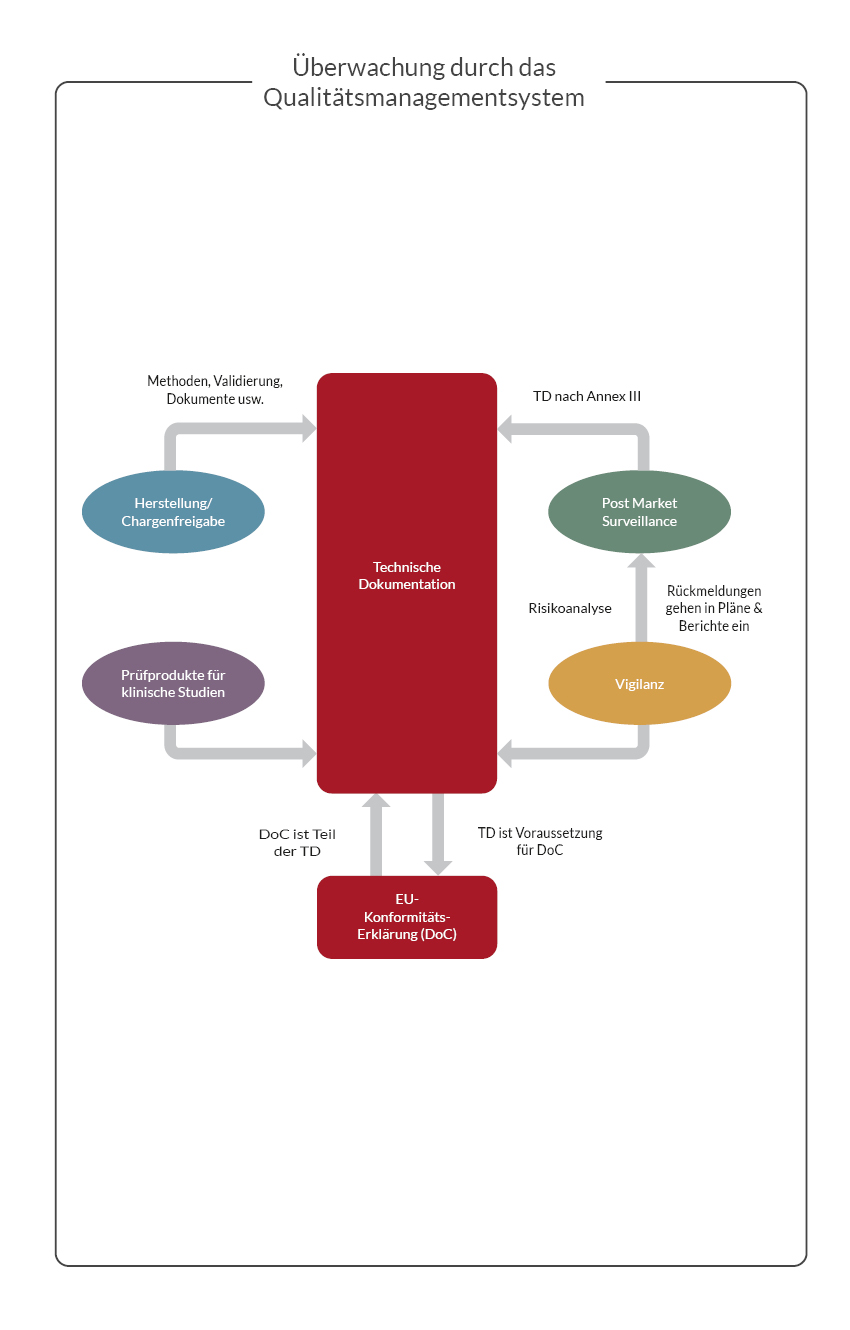
Hier obliegt es dem Hersteller zu entscheiden, ob es eine übergeordnete Verantwortliche Person geben soll, die alle Bereiche – wie Technische Dokumentation, Post-Market Surveillance, Vigilanz, Produktkonformität oder die Abgabe einer Erklärung für Prüfprodukte – überwacht oder ob für jeden Bereich eine eigene Verantwortliche Person benannt werden soll. Ebenfalls muss entschieden werden, ob die Verantwortliche Person die mit der Wahrnehmung der Verantwortung verbundenen Aufgaben alle selbst erfüllt oder ob die Ausführung delegiert wird und die Verantwortliche Person vorwiegend als Überwachungsorgan agiert. Sind diese Entscheidungen einmal getroffen, muss die neue Funktion der Verantwortlichen Person(en) inklusive der Verantwortungen und Aufgaben auch im Qualitätsmanagementsystem entsprechend abgebildet werden.
Bei einem EU-Repräsentanten unterscheidet sich die Verantwortlichen Person von der bei einem Hersteller. Die Verantwortliche Person übernimmt hier Verantwortungen und Aufgaben als Bindeglied zwischen EU und non-EU. Das Augenmerk liegt hier demzufolge weniger bei den Pflichten des Herstellers als bei der Sicherstellung von vollständiger und korrekter Dokumentation für den EU Markt sowie der Durchführung von notwendigen Registrierungen und der Kommunikation mit dem Hersteller und den kompetenten Behörden.
qtec als Ihr Partner
Es gibt keinen vorgeschriebenen Weg für die Implementierung einer Verantwortlichen Person. Jedoch muss gewährleistet sein, dass die Verantwortliche Person dieser Verpflichtung auch nachkommen kann. Bei der Implementierung der Verantwortlichen Person sollten das Unternehmen und die vorhandenen Strukturen individuell betrachtet werden, um eine passende Strategie zu entwickeln.
Für Hersteller und EU-Repräsentanten, die der Definition von Klein- und Kleinstunternehmen entsprechen, bietet wir zukünftig die Möglichkeit, zur Erfüllung der Verpflichtungen auf die qtec Expertinnen und Experten als externe Verantwortliche Person zuzugreifen. Wir entwickeln mit Ihnen eine passende Strategie und geben Hilfestellungen für die Umsetzung der folgende Punkte:
- Eine oder mehrere Verantwortliche Personen?
- Wie kann die Verantwortliche Person ihrer Verantwortung nachkommen und was kann delegiert werden?
- Übernahme der Verantwortungen durch die externe Verantwortliche Person für einen, mehrere oder alle Teilbereiche
- Erstellung eines Prozesses, wie der Verantwortung nachgekommen wird
- Überprüfung der relevanten QM Prozesse
- Überprüfung der Dokumentation
- Erstellung einer QSV
Wir können helfen!
Folgen Sie uns auf diesen Seiten und wir zeigen Ihnen, wie wir Sie unterstützen können. Und nutzen Sie gern unsere kostenlosen Angebote wie