
Nanopartikel und Nanomaterialien in der Medizintechnik
Nanostrukturen können einem Material neuartige Eigenschaften verleihen. Nanopartikel haben, im Verhältnis zum Gewicht oder Volumen, eine große Oberfläche. Nanodisperse Stoffe haben ein großes Potenzial, um die biologische Verfügbarkeit von Arzneimitteln und Diagnostika zu verbessern. Für therapeutische Zwecke gibt es bereits vielfältige Ansatzmöglichkeiten, die in Forschung und Entwicklung verfolgt werden 1, 2, 3.
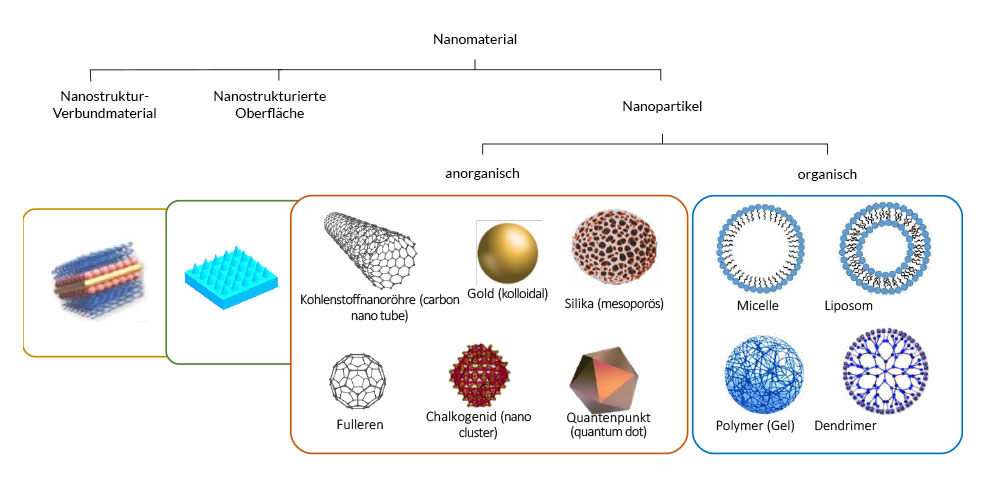
Nanomaterialien: Einsatz und Anwendungsbereich
Nanomedikamente sind derzeit noch im Entwicklungsstadium. Dabei konzentriert sich die Forschung auf Wirkstofftransportsysteme in Form von Mizellen, Liposomen und Dendrimeren 4 – vorwiegend mit dem Ziel der Tumorbekämpfung. Auch in Diagnostika bestehen Einsatzmöglichkeiten (z.B. Kontrastmittel). Nanostrukturierte Oberflächen sind bei Implantaten bereits im Einsatz, um beispielsweise das Einwachsverhalten zu verbessern. In der Therapie findet man unter anderem Hydroxyapatit-Nanopulver zur Füllung von Knochenlücken oder polymeres Bindematerial mit Nanopartikeln für Zahnzement. In einigen Verbrauchsgütern haben Nanomaterialien bereits Einzug gehalten 5, 6. In welchem Maß die Produkte durch Abbau für Mensch und Umwelt schädlich sein können, ist derzeit noch in Erforschung 7, 8.Seit 2013 gilt in der EU eine Kennzeichnungspflicht für Nanopartikel in Kosmetika und seit 2014 für Lebensmittel. Als kritisch zu bewerten sind Silber-Beschichtungen von Textilien oder Silber-Nanopartikel in Deodorants.
Nanomaterialien: Wirkungsweisen und Gefahren
Die Eigenschaften, die Nanomaterialien für die Produktentwicklung und die Arzneimittelabgabe potenziell vorteilhaft machen – wie Größe, Form und hohe Reaktivität – sind dieselben Eigenschaften, die Bedenken hinsichtlich der Art ihrer Wechselwirkung mit biologischen Systemen und möglicher Auswirkungen auf die Umwelt hervorrufen.
Die Wechselwirkungen des Körpers mit hergestellten Nanopartikeln können auch negative gesundheitliche Auswirkungen haben. Durch Freisetzung von Nanomaterialien in die Luft könnten noch feinere Aerosole die Belastung der Umwelt erhöhen. Man unterscheidet bei der Grenzwertfestlegung neben dem toxischen Potenzial des Materials auch die Eindringtiefe in die Atemwege, für die die Größenverteilung der Partikel ausschlaggebend ist. Die Arbeitsplatzgrenzwerte für einatembaren Staub aus allgemein biologisch unbedenklichem Material liegen bei 10 mg/m, für alveolengängigen, typischen Staub bei 1,25 mg/m³ und für Metalloxide bei 20 000 Partikeln/m³. Das heißt, die Arbeitsplatzgrenzwerte (AGW) und Derived No Effect Level (DNEL) sind dichte- und materialabhängig 9.
Wenn größere Mengen in die Umwelt gelangen, sind Probleme zu erwarten – besonders, wenn die Stoffe mobilisiert werden, lungen- oder kiemengängig sind und / oder sich anreichern können. Die Gefahr, dass Nanopartikel aus Cremes und Lotionen über die Atemwege in den Körper gelangen, ist generell als gering anzusehen.
Regularien für Nanomaterialien
Die Europäische Kommission definiert, dass ein Nanomaterial mindestens zur Hälfte aus Partikeln im Bereich von 1 bis 100 nm besteht 10. Nanomaterialien unterliegen der REACH- und CLP-Verordnung und sind somit registrierungspflichtig 11 und kennzeichnungspflichtig 12. Auch die Biozid-Verordnung macht Auflagen, wenn solche Stoffe verwendet werden. Produkte mit Nanomaterialien sind vom vereinfachten Zulassungsverfahren ausgeschlossen 13. Die FDA hat mehrere Richtlinien für Nanopartikel in Nahrungs-, Genuss- und Arzneimitteln veröffentlicht 14.
Besuchen Sie unsere BioLogisch Tagung in Stuttgart!
In dieser zweitägigen Konferenz am 18.03.-19.03.2026 erweitern Sie Ihr Fachwissen im Bereich Biologische Beurteilung und treten mit Benannten Stellen, Behörden und anderen Herstellern in den direkten Kontakt.
Risikobewertung
Das Risiko einer Gefährdung steigt mit der Möglichkeit einer Freisetzung von Nanopartikeln, sofern diese nicht beabsichtigt ist (wie z.B. bei dispergierten Arzneimitteln). An einer Oberfläche lassen sich adhärierenden Nanopartikel (z.B. Silberpartikel als antibiotische Beschichtung) leichter herauslösen als eingebettete (z.B. Füllstoff in Polymermatrix). Bei der Risikobewertung sind folglich neben der Materialart auch die Struktur und die Darreichungsform zu berücksichtigen.
Die MDR hat dies bei den Klassifizierungsregeln (Regel 19) berücksichtigt. Ein Hersteller hat mit der Inverkehrbringung die Pflicht, das toxikologische Profil, die Sicherheitsdaten und die Expositionsbedingungen des Nanomaterials anzugeben. Die OECD hat Tests und Methoden beschrieben, um das Risiko für solche Stoffe zu ermitteln15.
Update vom 03.09.2025
Unsere Fortbildungen
Sie möchten mehr erfahren? Dann buchen Sie das passende Seminar zum Thema. Oder benötigen sie eine Inhouse-Schulung? Dann kontaktieren Sie uns gerne unter academy@qtec-group.com
Referenzen
1 I. Uddin, S. Venkatachalam, A. Mukhopadhyay, M.A. Usmani: Nanomaterials in the Pharmaceuticals: Occurrence, Behaviour and Applications, Curr Pharm Des. 2016; 22(11):1472-84
2 X. Wang, L.H. Liu, O. Ramström O, M. Yan: Engineering nanomaterial surfaces for biomedical applications. Exp Biol Med (Maywood). 2009; 234(10):1128-39
3 Nanostructures and Nanomaterials: Synthesis, Properties, and Applications, Band 2 von World Scientific series in nanoscience and nanotechnology, C. Guozhong, W. Ying (Herausg.), World Scientific, 2011
4 A. C. Silva, C. M. Lopes, J.M.S. Lobo, M. H. Amaral: Delivery systems for biopharmaceuticals. Part II: Liposomes, Micelles, Microemulsions and Dendrimers, Current Pharmaceutical Biotechnology, 16 (11): 955 - 965, 2015
5 www.nanopartikel.info/nanoinfo/wissens-datenbank
6 www.nist.gov/programs-projects/nanomaterials-consumer-products
7 Nanomaterials: Risks and Benefits, NATO Science for Peace and Security Series C: Environmental Security, I. Linkov, J. A. Steevens (Hrsg.), Springer Science & Business Media, 2008
8 P.J.A. Borm, D. Robbins, S. Haubold, T. Kuhlbusch, H. Fissan, K. Donaldson, R. Schins, V. Stone, W. Kreyling, J. Lademann, J. Krutmann, D. Warheit, E. Oberdorster: The potential risks of nanomaterials: a review carried out for ECETOC; Part Fibre Toxicol. 2006; 3: 11
9 Technische Regel für Gefahrstoffe - TRGS 900 Arbeitsplatzgrenzwerte, Bundesanstalt für Arbeitsschutz und Arbeitssicherheit, Stand 2020
10 2011/696/EU: Recommendation on the definition of a nanomaterial, 2011
11 Appendix for nanoforms applicable to the Guidance on Registration and Substance Identification, ECHA, 2019
12 The applicability of the GHS classification criteria to nanomaterials, Nordisk Council of Ministers, 2019
13 EU-Verordnung 528/2012 über die Bereitstellung auf dem Markt und die Verwendung von Biozidprodukten (BPR), Stand 2012
14 Drug Products, Including Biological Products, that Contain Nanomaterials, Guidance for Industry, FDA, 2017
15 www.oecd.org/chemicalsafety/nanosafety/testing-programme-manufactured-nanomaterials










